- Dr Pierre Carvelli, Médecin spécialiste en formationGynécologie-Obstétrique
- Dr Emilien Grégoire, Infectiologue
- Pr Michelle Nisolle, Chef de service, service universitaire de Gynécologie-Obstétrique
- Dr Jean-Marc Senterre, Chef de Service AdjointBiologie clinique
Les infections génitales hautes (IGH)
On retrouve les endo-métrites, les infections tubaires (salpingites) et les collections purulentes pelviennes caractérisant les formes compliquées : pyosalpinx, abcès tubo-ovariens, et pelvipéritonites. Les endocervicites sont souvent le point de départ, font anatomiquement partie des IGH et résultent habituellement d’une contamination par voie ascendante.(1)
Étiologies
La contamination se fait quasi exclusivement par voie génitale ascendante. On distingue les germes sexuellement transmissibles de ceux issus de la flore vaginale et des infections nosocomiales.
Principaux germes transmis sexuellement :
_ Chlamydia trachomatis (CT) : le risque de développer une IGH à partir d’une chlamydiose urogénitale basse est mal connu(2)
20 % des femmes ainsi atteintes feraient une IGH,
3 % développeraient une stérilité séquellaire, CT étant le pathogène potentiellement le plus délétère pour les trompes de Fallope,
2 % une grossesse extra-utérine (GEU).
_ Gonocoque : Neisseria gonorrhoeae (NG) est un diplocoque à Gram négatif très contagieux infectant essentiellement chez la femme le col utérin.
_ Mycoplasma genitalium : (MG) jamais présent à l’état commensal dans la flore vaginale.(3)
Les autres germes : les aérobies, les entérobactéries, les streptocoques
Diagnostic d’une infection génitale haute
_ Signes fonctionnels et anamnèse : douleurs pelviennes, leucorrhées, douleurs de l’hypocondre, fièvre (rare en cas d’IGH non compliquée, >38.5, il faut rechercher un IGH compliqué), métrorragie, dyspareunie, signes urinaires, syndrome rectal. Recherche des facteurs favorisants : antécédents d’IST, activité sexuelle, mode de contraception, DIU, acte chirurgical, exploration endo-utérine, accouchement récent.
_ Le diagnostic clinique d’une IGH non compliquée est souvent difficile : au spéculum, il existe souvent une cervicite. Le toucher vaginal révèle une douleur lors de la palpation et mobilisation utérine et/ou annexielle.
_ Examens complémentaires :
Microbiologique : indispensable ; consiste en un prélèvement endovaginal (recherche par PCR de CT, NG et MG + examen direct).
Examen biologique : l’hyperleucocytose est plus souvent retrouvée dans les formes compliquées. La CRP est souvent majorée et son taux est corrélé à la sévérité de l’IGH.
Imagerie :
Échographie : plus sensible pour les formes compliquées. On retrouve des critères d’IGH : paroi tubaire, franges épaissies, aspect tubaire en roue dentée, abcès tuboovarien et un épanchement péritonéal. Examen de première ligne intéressant mais peu sensible.
Tomodensitométrie abdomino-pelvien : utile dans le cadre des urgences pour les formes compliquées pour distinguer une autre origine de l’infection.
Coelioscopie diagnostique : permet de faire le diagnostic, de caractériser le type d’IGH, de faire les prélèvements bactériologiques et de donner un pronostic en constatant les adhérences déjà présentes et l’état des trompes. Elle permet des gestes thérapeutiques : drainage de la charge bactérienne, lever les adhérences... Mais elle n’aide pas au diagnostic des endométrites et salpingites et s’accompagne d’un risque de morbi-mortalité. Donc le recours à la coelioscopie ne doit pas être systématique pour les formes non compliquées.
Le Collège National des Gynécologues et Obstétriciens Français (CNGOF) a publié des recommandations pour la pratique clinique qui comprennent un modèle diagnostique des IGH basé sur l’interrogatoire, l’examen clinique et l’échographie(4). Ce modèle est basé sur la présence d’un des deux critères majeurs de l’examen clinique que sont la douleur à la mobilisation utérine et la douleur annexielle provoquée.
Traitement et prise en charge
Pour les formes non compliquées, le traitement doit être débuté sur base clinique dès la suspicion évoquée pour limiter le risque de séquelles : stérilité tubaire, GEU, douleur pelvienne chronique.(5)
Une thérapie à large spectre, qui doit couvrir le chlamydia trachomatis, le neisseria gonorrhoeae, les anaérobies, les entérobactéries, les streptocoques et le mycoplasme genitalium, est administrée en ambulatoire.
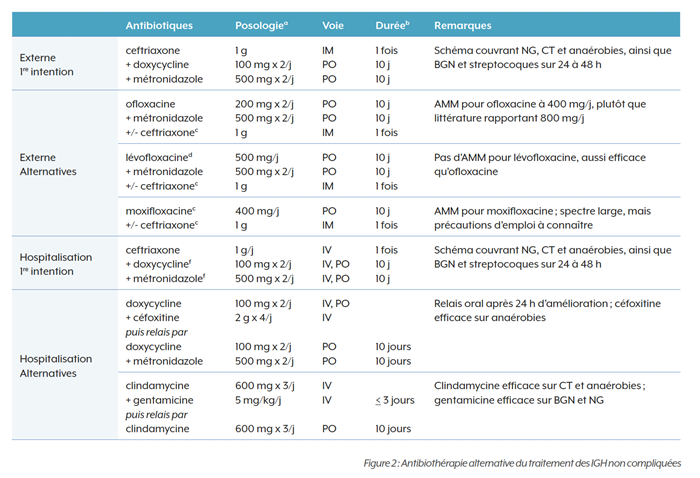
Schéma antibiotique(6-7) (alternatives Figure 2) :
_ Ceftriaxone 500mg ou 1g IM 1 dose,
_ Doxycycline 100mg 2x/J P,10/14 jours,
_ Métronidazole 500mg 2x/J PO 10/14 jours,
_ Réévaluation à J3-J5 : évolution clinique, qualité de l’observance, résultat microbiologique et adaptation du traitement si germe retrouvé.
Traitement du partenaire :
Le traitement du partenaire est systématique en cas d’infection à germe sexuellement transmissible. En cas de chlamydiose, l’azithromycine monodose (1g en une prise unique). En cas de gonococcie, compte tenu des recommandations actuelles, injection intramusculaire de 500mg de ceftriaxone. Rapports sexuels protégés pendant 10 à 15 jours et jusque résolution des symptômes de PID.
Critères d’hospitalisation(5) :
Incertitude diagnostique, sévérité de la présentation clinique (sepsis, intensité des douleurs), présence ou suspicion d’abcès tubo-ovarien, signes digestifs faisant anticiper une difficulté de prise orale, situation psychologique ou sociale faisant craindre une inobservance, grossesse, échec de traitement oral, patiente, immunodéprimée.
Suivi des patientes :
Le taux de récidive est de 15-21 % avec un haut taux de réinfection, diminué par un suivi adéquat.
Potentielles complications à long terme : infertilité, douleur pelvienne chronique (30 %), risque de GEU. Toutes les patientes présentant un IGH doivent être testées pour chlamydia, gonocoque (mycoplasme genitalium), HIV, hépatites et syphilis.
Il est intéressant de prélever un frottis vaginal après 3-6 mois (germe banal), avant insertion d’un DIU, avant une IVG ou avant une hystéro-salpingographie. Une PCR vaginale 3 à 6 mois après une IGH due à une IST est proposée pour éliminer une infection persistante ou une réinfection.
Take home messages :
_ Les signes d’appel d’IGH doivent conduire à un examen clinique gynécologique, un prélèvement vaginal microbiologique et une échographique gynécologique.
_ Sans critère d’hospitalisation et sur base clinique, un traitement large spectre est mis en place.
_ Les résultats microbiologiques orientent l’antibiothérapie et la nécessité de traiter le partenaire.
_ Ce traitement et un suivi approprié permettent d’éviter un bon nombre de complications : abcès tubo-ovariens, infertilité, GEU et douleurs chroniques pelviennes.
(1) Bouquier J, Fauconnier A, Fraser W, Dumont A, Huchon C. Diagnostic d’une infection génitale haute. Quels critères cliniques, paracliniques ? Place de l’imagerie et de la coelioscopie ? J Obstet Gynecol Obstet Biol Reprod 2012 ;41 :835 49.
(2) Paavonen J, Eggert-Kruse W. C. trachomatis : impact on human reproduction. Hum Reprod Update 1999 ;5 :433–7.
(3) De Barbeyrac B, Bernet-Poggi C, Febrer F, Renaudin H, Dupon M, Bébéar C. Detection of M. pneumoniae and M. genitalium by polymerase chain reaction in clinical samples. Clin Infect Dis 1993 ;17(Suppl. 1) :S83–9.
(4) Judlin P, Huchon C, Quentin R, Bourret A, Garbin O, Derniaux E, et al. Infections génitales hautes. EMC - Gynécologie 2015 ;10(4) :1-16 [Article 470-A-10].
(5) Gynecol Obstet Fertil Senol 2019. J-L Brun et al.
(6) 1.Kimberly A. Workowski et al. Sexually Transmitted Infections Treatment Guidelines, 2021 . MMWR Recomm Rep 2021 ;70(No. 4)
(7) 1.Savaris RF, Fuhrich DG, Maissiat J, Duarte RV, Ross J. Antibiotic therapy for pelvic inflammatory disease. Cochrane Database Syst Rev. 2020 Aug 20 ;8(8) :CD010285. doi : 10.1002/14651858.CD010285.pub3. PMID : 32820536 ; PMCID : PMC8094882.